任務3.3 認識稀溶液依數性及其應用
3.3.1 任務書
溶液的某些性質,只與溶液中溶質粒子的多少有關,而與溶質的本性無關,這類性質通常稱為溶液的依數性,主要有溶液的蒸氣壓下降、沸點升高、凝固點降低以及溶液具有滲透壓。本次任務要求學生利用凝固點降低法測定葡萄糖的摩爾質量,理解溶液依數性的應用,掌握凝固點測量技術,并掌握固體的稱量、液體量取、一般溶液配制等基本操作技能。
3.3.2 技能訓練和解析 凝固點降低法測定物質相對分子質量實驗
1.操作原理
凝固點是溶液與其固態溶劑具有相同的蒸氣壓而能平衡共存時的溫度。當在溶劑中加入難揮發的非電解質溶質時,由于溶液的蒸氣壓小于同溫度下純溶劑的蒸氣壓,因此溶液的凝固點必定小于純溶劑的凝固點。按照圖3-3連接裝置測定溶液的凝固點。
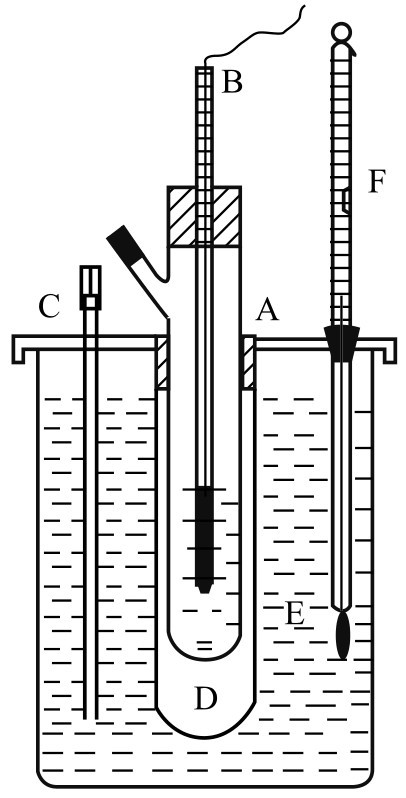
圖3-3 溶液凝固點測定裝置
A—冷凍管;B—貝克曼溫度計;C—攪拌器;D—外套管;E—冰水浴;F—溫度計
根據拉烏爾定律可推出:稀溶液的凝固點降低值ΔTf近似地與溶液的質量摩爾濃度成正比,而與溶質的本性無關,即: ,式中,ΔTf表示溶液凝固點的降低值;Tf表示溶液的凝固點;
,式中,ΔTf表示溶液凝固點的降低值;Tf表示溶液的凝固點; 表示純溶劑的凝固點;bB表示溶液的質量摩爾濃度(溶液中,溶質的物質的量與溶劑質量的比值稱為質量摩爾濃度,單位為mol/kg);Kf表示溶劑的凝固點下降常數,單位是K·kg/mol,它是溶劑的特征常數,隨溶劑的不同而不同。
表示純溶劑的凝固點;bB表示溶液的質量摩爾濃度(溶液中,溶質的物質的量與溶劑質量的比值稱為質量摩爾濃度,單位為mol/kg);Kf表示溶劑的凝固點下降常數,單位是K·kg/mol,它是溶劑的特征常數,隨溶劑的不同而不同。
由此可導出計算溶質摩爾質量MB的公式:MB= ,因此,在已知Kf、溶劑質量、溶質質量的前提下,只要測出溶液的凝固點降低值ΔTf,即可求出溶質的摩爾質量和相對分子質量。
,因此,在已知Kf、溶劑質量、溶質質量的前提下,只要測出溶液的凝固點降低值ΔTf,即可求出溶質的摩爾質量和相對分子質量。
通常測定凝固點的方法是將溶液逐漸冷卻,使其結晶。但是,實際上溶液冷卻到凝固點,往往并不析出晶體,這是因為新相形成需要一定能量,故結晶并不析出,這就是所謂過冷現象。然后由于攪拌或加入晶種促使溶劑結晶,由結晶放出凝固熱,使體系溫度回升,并保持相對穩定,直至全部液體凝固后溫度下降,這一過程中相對穩定的溫度就是該溶液的凝固點。
2.任務材料

3.任務操作
(1)純溶劑凝固點的測定

(2)葡萄糖溶液的凝固點測定


4.記錄與報告單(見表3-6)
表3-6 葡萄糖相對分子質量測定數據記錄與結果
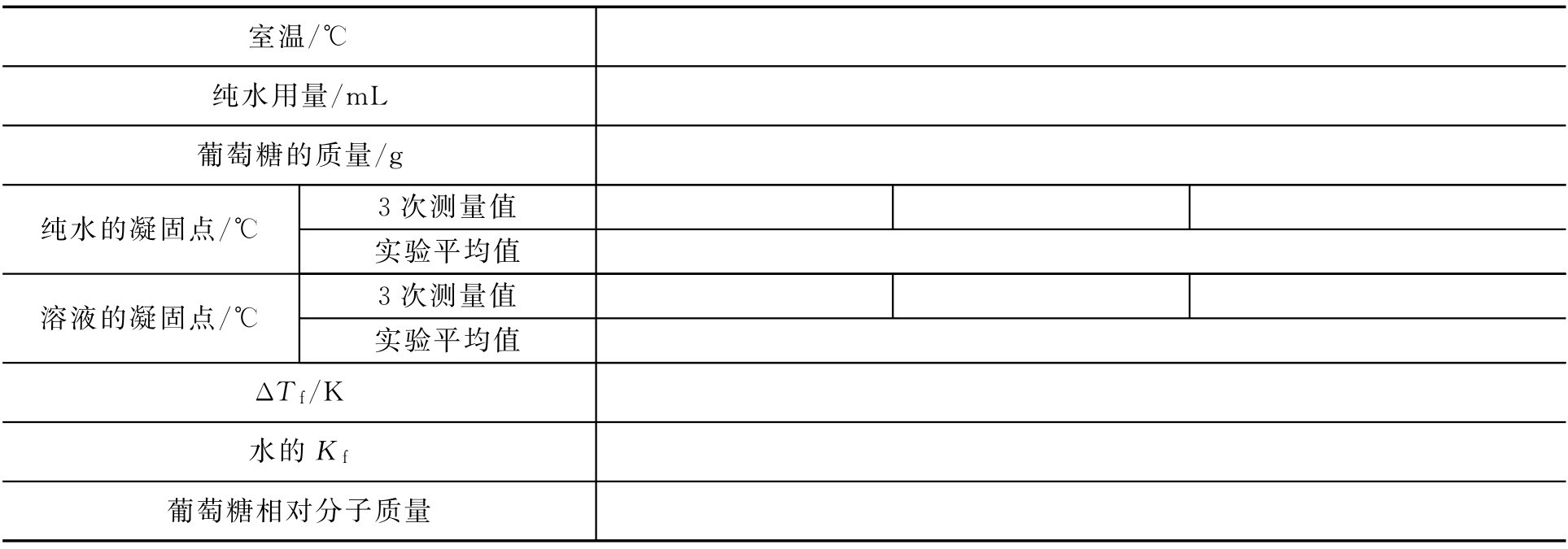
實驗結論:
稀溶液的依數性主要有________、________、________和________,測定某物質的摩爾質量可采用________法。
3.3.3 知識寶庫 一般稀溶液的性質
溶液的性質分為兩類:一類是與溶液的本性及溶質與溶劑的相互作用有關,如顏色、酸堿性和導電性等;另一類是只與溶液中溶質粒子的多少有關,而與溶質的本性無關,這類性質通常稱為溶液的依數性,主要有:溶液的蒸氣壓下降、沸點升高、凝固點降低以及溶液的滲透壓。人們在討論溶液的依數性時,通常是指難揮發性非電解質的稀溶液,不考慮溶液中粒子間的相互作用。
1.溶液的蒸氣壓下降
蒸發是指在一定溫度下,將一杯純水放在密閉的容器中,由于分子的熱運動,一部分能量較高的水分子從水面逸出,擴散到空氣中形成水蒸氣的過程;凝結是指水蒸氣分子在不斷運動的過程中,其中一些分子又重新回到水面變成液態水的過程。

當蒸發速率與凝結速率相等時,氣相和液相達到動態平衡,水面上的蒸氣壓保持不變,此時的蒸氣壓稱為該溫度下純水的飽和蒸氣壓,簡稱蒸氣壓,單位為kPa。
在同一溫度下,由于加入溶質時,溶液中單位體積溶劑蒸發的分子數目降低,逸出液面的溶劑分子數目相應減少,因此在較低的蒸氣壓下建立平衡,即溶液的蒸氣壓比純溶劑的蒸氣壓低(p0-p),這就是溶液的蒸氣壓下降,如圖3-4所示。
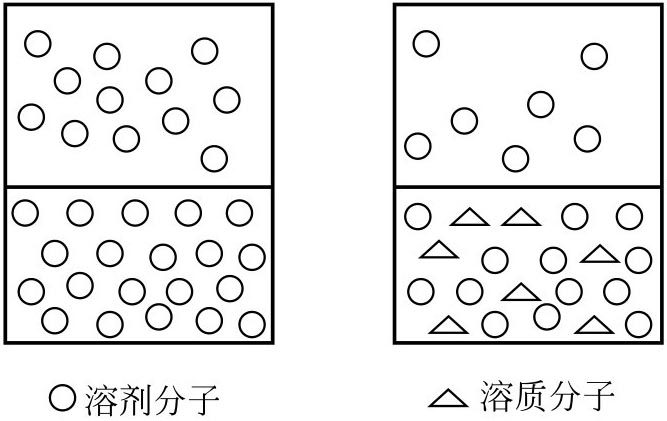
圖3-4 溶液的蒸氣壓下降
因此,在液體中加入任何一種難揮發性非電解質,液體的蒸氣壓就下降,純溶劑蒸氣壓與溶液的蒸氣壓的差值用Δp表示:
Δp=p0-p (3-11)
式中,Δp表示溶液蒸氣壓的下降值Pa或kPa;p0表示純溶劑的蒸氣壓;p表示溶液的蒸氣壓。
在一定溫度下,難揮發非電解質稀溶液的蒸氣壓下降與該溶液的質量摩爾濃度成正比,此為拉烏爾定律。即:
Δp=KbB (3-12)
式中,bB為溶液的質量摩爾濃度;K為比例常數。
該式表明,在一定溫度下,難揮發性非電解質稀溶液的蒸氣壓下降Δp只與溶液的質量摩爾濃度有關,而與溶質的種類和本性無關。若有質量摩爾濃度相同的幾種非電解質稀溶液,如葡萄糖溶液、蔗糖溶液、尿素溶液,其蒸氣壓的降低值則是相等的。
2.溶液的沸點升高
液體(純液體或溶液)的蒸氣壓隨溫度的升高而增大,當液體的蒸氣壓與外界壓強相等時的溫度,即稱為該液體的沸點。若未指明外界壓強,則一般認為外界壓強是一個標準大氣壓。
對于難揮發性非電解質的稀溶液,由于其蒸氣壓下降,要使溶液蒸氣壓達到與外界壓強相等,就要使其升高溫度超過純溶劑的沸點。因此,非電解質稀溶液的沸點要比純溶劑的沸點高,如圖3-5所示。
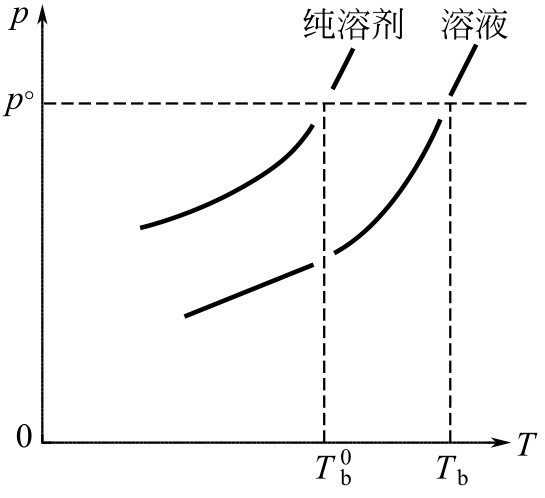
圖3-5 溶液的沸點升高
溶液沸點升高是由于溶液的蒸氣壓下降導致的,而溶液的蒸氣壓下降程度與溶液的質量摩爾濃度成正比,因此,溶液沸點的升高程度也與其質量摩爾濃度成正比,而與溶質的本性無關,且溶液的濃度越大,其沸點越高。即:

式中,ΔTb表示溶液沸點的升高值;Tb表示溶液的沸點; 表示純溶劑的沸點;bB表示溶液的質量摩爾濃度;Kb表示溶劑的沸點升高常數,K·kg/mol,它隨溶劑的不同而不同,見表3-7。
表示純溶劑的沸點;bB表示溶液的質量摩爾濃度;Kb表示溶劑的沸點升高常數,K·kg/mol,它隨溶劑的不同而不同,見表3-7。
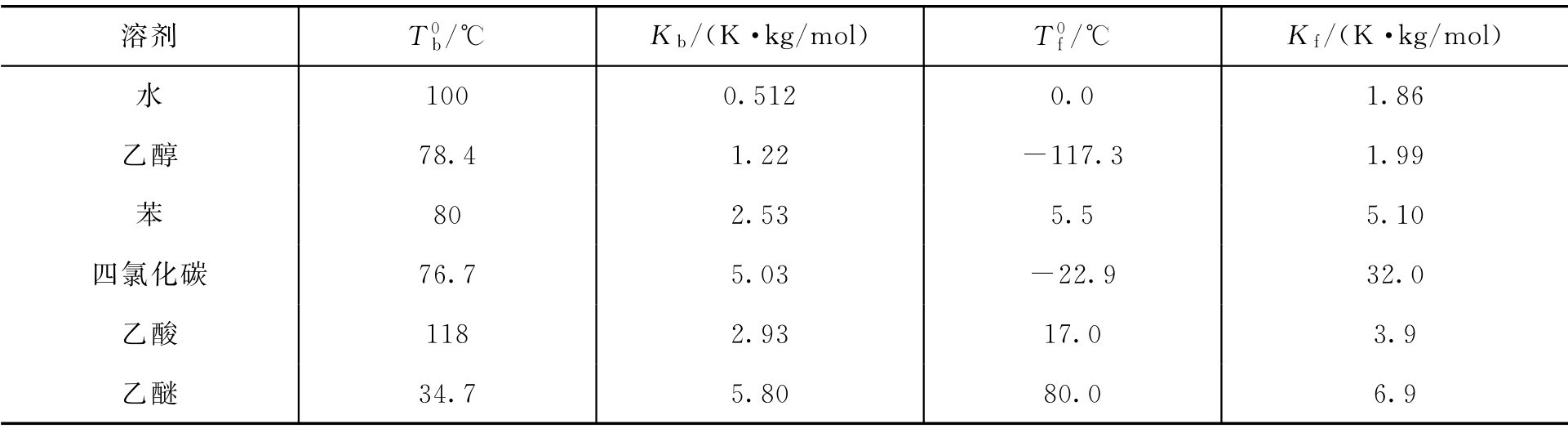
表3-7 常見溶劑的 、Kb和
、Kb和 、Kf值
、Kf值
3.溶液的凝固點下降
溶劑的凝固點是物質的液相和固相平衡共存時的溫度。達到凝固點時,液、固兩相的蒸氣壓相等,否則兩相不能共存。例如,純水的凝固點為0℃(即273.15K),此時水和冰的蒸氣壓相等,均為610.6Pa。溶液的凝固點是指溶液液相和固態溶劑平衡共存時的溫度。溶液的凝固點比純溶劑的凝固點低,如圖3-6所示。溶液的濃度越大,凝固點就越低。
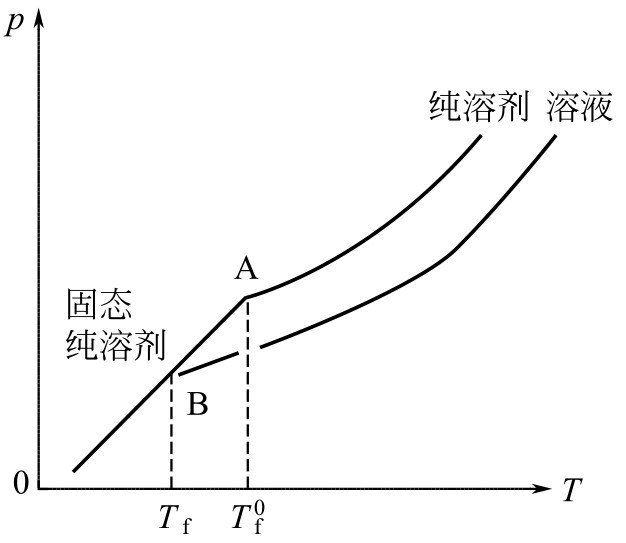
圖3-6 溶液的凝固點降低
溶液的凝固點下降也是由于其蒸氣壓下降的緣故,因此,溶液凝固點的下降程度也只與溶液濃度有關,而與溶質的本性無關。溶液凝固點的下降值與溶液的質量摩爾濃度成正比,且溶液濃度越大,其凝固點越低。即:

式中,ΔTf表示溶液凝固點的降低值;Tf表示溶液的凝固點; 表示純溶劑的凝固點;bB表示溶液的質量摩爾濃度;Kf表示溶劑的凝固點下降常數,K·kg/mol,它是溶劑的特征常數,隨溶劑的不同而不同,見表3-7。
表示純溶劑的凝固點;bB表示溶液的質量摩爾濃度;Kf表示溶劑的凝固點下降常數,K·kg/mol,它是溶劑的特征常數,隨溶劑的不同而不同,見表3-7。
溶液凝固點下降的性質在多種領域得到廣泛應用。例如,冬天在汽車水箱里加入乙二醇或甘油可以起到防凍作用;在冰中加入鹽可用作制冷劑;可根據溶液凝固點降低的性質測定某未知物的相對分子質量等。
4.溶液的滲透壓
凡是溶液都具有滲透壓,這是溶液的一個重要性質。溶液的滲透壓在生物、醫學等方面有廣泛應用,如臨床上給病人補充液體時要密切注意溶液的濃度,過濃或過稀都將產生不良后果,甚至造成死亡,這與溶液的滲透壓有著密切的聯系。
(1)滲透現象和滲透壓
若在一杯清水中小心加入一層濃蔗糖水,不久整杯水都有甜味;若在一杯清水中滴入一滴紅墨水,不久整杯水都變為紅色。這是由于蔗糖分子從上層進入下層,同時水分子從下層進入上層,直到整杯溶液的濃度均勻為止,這種在兩種不同濃度的溶液之間,由于溶質分子和溶劑分子無規則運動而相互分布的現象稱為擴散。擴散是一種雙向運動,只要兩種不同濃度的溶液相互接觸,就會發生擴散現象。
如果將蔗糖溶液與清水用理想半透膜(半透膜是一種具有選擇性的薄膜,它只允許溶劑分子透過,而不允許溶質分子透過,例如細胞膜、動物的膀胱膜、人造羊皮紙和火棉膠膜等)隔開,并使膜兩側的液面相平,靜置一段時間后,可以看到蔗糖溶液一側的液面升高,如圖3-7所示。我們把這種溶劑分子自發地通過半透膜,由純溶劑溶液進入溶液,或由低濃度溶液進入高濃度溶液的現象稱為滲透現象,簡稱滲透。
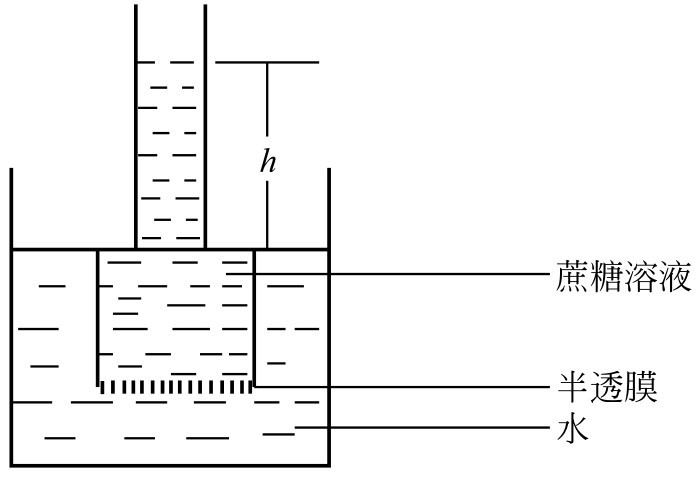
圖3-7 溶液的滲透現象和滲透壓
滲透是特殊條件下的擴散現象。滲透現象的產生必須具備以下兩個條件:一是必須存在半透膜;二是半透膜兩側溶液存在一定的濃度差。
滲透現象的產生是由于蔗糖分子不能透過半透膜,而水分子卻可以自由地透過半透膜。由于膜兩側單位體積內的水分子數目不相等,單位時間內水分子從純水(或稀溶液)進入蔗糖溶液(或濃溶液)的數目比蔗糖溶液中水分子在同一時間內進入純水(或稀溶液)的數目多,其結果是蔗糖溶液的液面升高,濃度降低。隨著溶液液面的升高,由溶液液柱產生的靜水壓促使溶液中的水分子加速向純水中擴散,當溶液液面上升到一定高度時,兩種反向的擴散速率相等,此時,單位時間內從膜兩側透過的水分子數目相等,從而形成了一種動態平衡,溶液液面不再升高,這種動態平衡稱為滲透平衡。
滲透的凈方向總是趨于自發縮小膜兩側溶液的濃度差,亦即滲透總是溶劑分子從純溶劑一側進入溶液一側,或從稀溶液一側進入濃溶液一側。
為了使半透膜兩側液面的高度相等并保持不變,必須在溶液液面上施加一額外壓力。這種為維持溶液和溶劑之間的滲透平衡而需要的超額壓力稱為滲透壓。滲透壓用符號Π表示,單位是Pa或kPa。若在溶液液面上方施加的外壓大于滲透壓,則溶劑分子的滲透方向就會從溶液一側進入純溶劑一側,溶液液面降低,這種逆向進行的操作稱為反滲透。此技術常用于從海水中提取淡水和三廢治理中處理污水。
(2)滲透壓與濃度、溫度的關系
1886年,荷蘭化學家范特荷甫(Van't Hoff)根據實驗結果總結出以下規律:稀溶液的滲透壓與溶液的濃度和熱力學溫度的乘積成正比。這就是范特荷甫定律,用方程式表示即為:
Π=cRT (3-15)
式中,Π為溶液的滲透壓,kPa;c為溶液的濃度,mol/L;R為氣體常數,R=8.31kPa·L/(mol·K);T為熱力學溫度,T=273+t℃,K。
由上式可知,在一定溫度下,難揮發性非電解質稀溶液的滲透壓只與單位體積溶液中的溶質顆粒的數目成正比,而與溶質的本性無關。
在相同溫度下,任何非電解質溶液的物質的量濃度相同時,單位體積內溶質顆粒的數目就相等,因此,它們的滲透壓也必定相等。例如,0.30mol/L的葡萄糖溶液與0.30mol/L的蔗糖溶液的滲透壓相等。
對于電解質溶液,由于電解質在溶液中發生解離,單位體積內溶質顆粒的數目要比相同物質的量濃度的非電解質溶液多,因此,其滲透壓也增大。如相同物質的量濃度的NaCl溶液和葡萄糖溶液相比,NaCl溶液單位體積溶液中的溶質粒子數是葡萄糖溶液粒子數的2倍,其滲透壓也幾乎是葡萄糖溶液的2倍。因此,在計算電解質溶液的滲透壓時,必須在上述公式中引入一個校正因子i,即:
Π=icRT (3-16)
i是電解質的一個“分子”在溶液中產生的質點數,對強電解質稀溶液,可近似認為1mol強電解質解離產生的離子的物質的量。如NaCl的i是2,MgCl2的i是3。式(3-16)中的ic則是溶液中各種溶質粒子的總濃度。
(3)滲透濃度
由式(3-16)可知,在一定溫度下,溶液滲透壓的大小只與單位體積內溶液中溶質的粒子數目成正比。我們把溶液中這些產生滲透效應的溶質粒子(分子或離子)統稱為滲透活性物質,因此,可以用滲透活性物質的濃度來衡量溶液滲透壓的大小。我們將溶液中滲透活性物質的總濃度定義為滲透濃度,用符號cos表示,其常用單位為mmol/L。
對于任何稀溶液,當溫度一定時,其滲透壓與稀溶液的滲透濃度成正比。因此,醫學上常用滲透濃度來表示溶液滲透壓的大小。
【例3-2】計算生理鹽水(9.00g/L NaCl溶液)和50.0g/L葡萄糖溶液的滲透濃度。
解 生理鹽水溶質NaCl是強電解質,其i=2;葡萄糖為非電解質,其i=1。因此,其滲透濃度分別是:

(4)等滲、低滲和高滲溶液
相同溫度下,滲透壓或滲透濃度相等的兩種溶液稱為等滲溶液;滲透壓不等的溶液,其中滲透壓相對較高的稱為高滲溶液,滲透壓較低的則稱為低滲溶液。
在醫學上,通常以正常血漿的總滲透壓或總滲透濃度為比較標準來衡量等滲、低滲和高滲溶液。正常人血漿的總滲透壓為720~820kPa,相當于總滲透濃度為280~320mmol/L。因此,臨床規定凡是滲透濃度在280~320mmol/L范圍內的溶液稱為等滲溶液,低于280mmol/L的溶液稱為低滲溶液,高于320mmol/L的溶液稱為高滲溶液。如生理鹽水、50.0g/L葡萄糖溶液、19.0g/L乳酸鈉、12.5g/L碳酸氫鈉等溶液都是臨床上常用的等滲溶液。
臨床輸液時,應用等滲溶液是一個基本原則。生理情況下,人血漿的滲透壓與紅細胞內液是等滲的,因此,如果將血紅細胞放入低滲溶液中,在顯微鏡下可觀察到紅細胞逐漸膨脹、破裂,造成溶血;反之,若在靜脈補液時,大量輸入高滲溶液,則紅細胞內的水分子便透過細胞膜進入血漿,紅細胞發生皺縮,稱為胞漿分離,會導致紅細胞黏聚成團而發生血管栓塞。