任務2.1 認識化學反應速率的影響因素
2.1.1 任務書
本次技能訓練通過過二硫酸銨與碘化鉀的反應,完成下列任務:
①一定溫度下,測定過二硫酸銨與碘化鉀的反應速率,計算反應速率常數、反應的活化能和反應級數。
②測定不同溫度下的反應速率,計算反應的活化能。
③一定溫度下,測定催化劑Cu(NO3)2滴入量不同時的反應速率,計算反應的反應速率常數。
從而了解反應速率概念及表示方法,理解濃度、溫度和催化劑對反應速率的影響。
2.1.2 技能訓練和解析 化學反應速率的影響因素實驗
1.任務原理
(1)計算一定溫度下反應級數和反應速率常數
一定溫度下,水溶液中過二硫酸銨和碘化鉀發生式(2-1)反應,加入一定體積Na2S2O3溶液和淀粉溶液,同時還進行式(2-2)反應,如下:


反應式(2-2)進行得很快,幾乎瞬間完成,而反應式(2-1)比反應式(2-2)緩慢得多,所以由式(2-1)生成的碘立即與 反應,生成無色的
反應,生成無色的 和I-。因此,在反應的初始階段,溶液呈無色。但是,當Na2S2O3一旦耗盡,反應式(2-1)生成的微量碘就很快與淀粉作用,使溶液呈藍色。從式(2-1)和式(2-2)反應也可以得到:
和I-。因此,在反應的初始階段,溶液呈無色。但是,當Na2S2O3一旦耗盡,反應式(2-1)生成的微量碘就很快與淀粉作用,使溶液呈藍色。從式(2-1)和式(2-2)反應也可以得到:

一定溫度下,瞬時速率為:
平均速率為:
近似地用平均速率代替瞬時速率:

綜上所述,一定溫度下化學反應瞬時速率為:

由式(2-3),兩邊取對數,得:

當c(I-)不變,lgv對 作圖,可得一直線,斜率即為m。同理,保持
作圖,可得一直線,斜率即為m。同理,保持 不變,lgv對lgc(I-)作圖,可計算得n,從而得到反應級數m+n。通過m和n以及化學速率計算方程式(2-3),可以得到速率常數k。
不變,lgv對lgc(I-)作圖,可計算得n,從而得到反應級數m+n。通過m和n以及化學速率計算方程式(2-3),可以得到速率常數k。
(2)計算不同溫度下反應的活化能
利用阿侖尼烏斯方程:

求得不同溫度下的k,以lgk對1/T作圖得一直線,此直線的斜率為 ,由此可以計算反應活化能Ea。
,由此可以計算反應活化能Ea。
2.任務材料

3.任務操作
(1)濃度對化學反應速率的影響
按表2-1編號A中的藥品用量進行操作,如圖2-1所示。

圖2-1 濃度的影響實驗操作步驟示意圖
①加20.0mL KI(0.20mol/L)溶液與15.0mL(NH4)2SO4溶液。
②加8.0mL Na2S2O3(0.01mol/L)溶液。
③加2.0mL 0.2%淀粉溶液。
④倒入150mL燒杯中,混合均勻。
⑤5.0mL(NH4)2S2O8(0.20mol/L)溶液,迅速倒入上述混合液中。
⑥同時啟動秒表,并不斷攪動。
⑦當溶液剛出現藍色時,立即按停秒表,記錄反應時間和溫度。
將本任務操作的測定數據填入表2-1中。
用同樣方法進行表2-1中編號B~F操作,為了使每次操作中溶液的離子強度和總體積保持不變,所減少的KI用量可用KNO3來平衡,所減少的(NH4)2S2O8用量用(NH4)2SO4來平衡。
(2)溫度對化學反應速率的影響
①按表2-1編號F中的藥品用量操作,如圖2-2所示,取KI(10.0mL)、Na2S2O3(8.0mL)、KNO3(10.0mL)、淀粉溶液(2.0mL),混合于大燒杯中。
表2-1 濃度對反應速率的影響

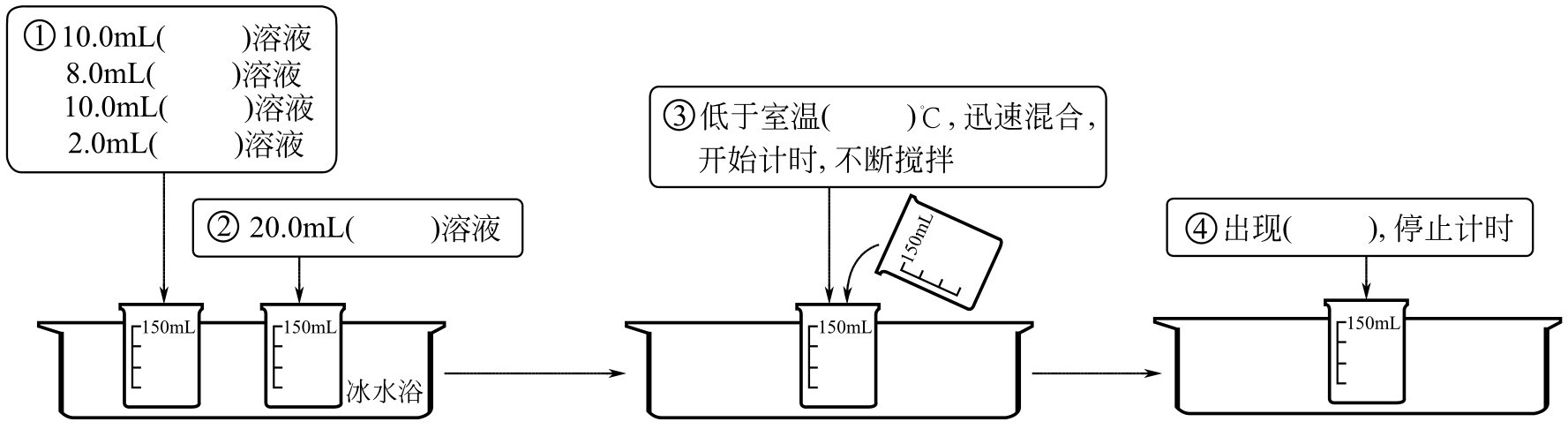
圖2-2 溫度的影響實驗操作步驟示意圖
②取20.0mL(NH4)2S2O8于小燒杯。
③大、小燒杯同時冰水浴,至低于室溫10℃時,迅速混合、計時并不斷攪拌。
④當溶液剛出現藍色時,記錄反應時間,此操作編號記為F1。
將本任務操作的測定數據填入表2-2中。
表2-2 溫度對化學反應速率的影響

同樣方法在熱水中進行高于室溫10℃的操作,此操作編號記為F2,將兩次操作數據F1、F2和操作F的數據記入表2-2中進行比較。
注意:不同溫度溫差一般控制在10℃,高溫不要超過30℃。
(3)催化劑對化學反應速率的影響
①按表2-1編號F中的藥品用量操作,如圖2-3所示,取KI(10.0mL)、Na2S2O3(8.0mL)、KNO3(10.0mL)、淀粉溶液(2.0mL)混合于150mL燒杯。
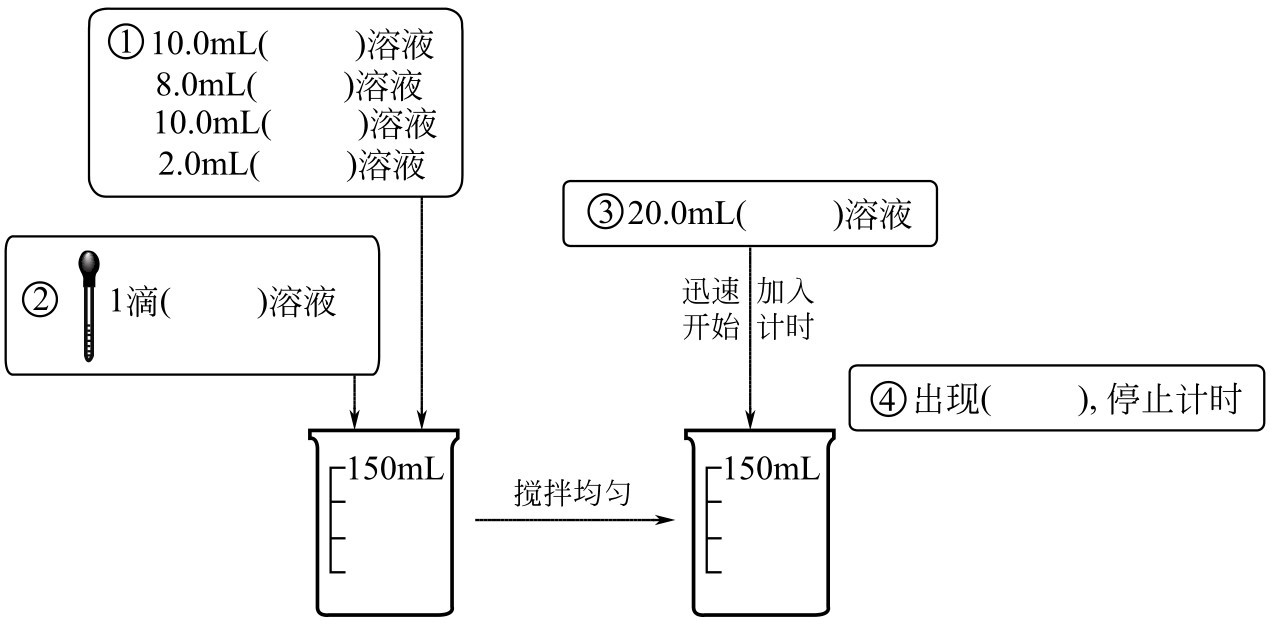
圖2-3 催化劑的影響實驗操作步驟示意圖
②加入1滴Cu(NO3)2溶液,攪勻。
③迅速加入20.0mL過二硫酸銨溶液,攪動、計時。
④當溶液剛出現藍色時,記錄反應時間。
將本任務操作的數據填入表2-3中,并分別再增加Cu(NO3)2催化劑用量至2滴及3滴。作同樣實驗后,將所得結果也填入表2-3中。
表2-3 催化劑對反應速率的影響
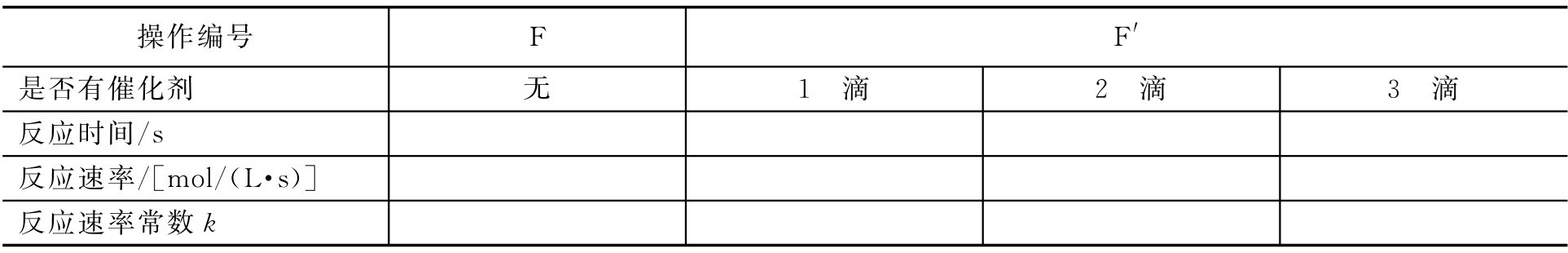
4.注意事項
本操作對試劑有一定的要求。碘化鉀溶液應為無色透明溶液,不宜使用有碘析出的淺黃色溶液。過二硫酸銨溶液要新配制,因為時間長過二硫酸銨易分解。如所配制過二硫酸銨溶液的pH小于3,說明該試劑已分解,不適合本操作使用。所用試劑中如混有少量Cu2+、Fe3+等雜質,對反應會有催化作用,必要時需滴入幾滴0.10mol/L EDTA溶液。
5.記錄與報告單
(1)數據記錄
(2)數據計算
①反應級數和反應速率常數的計算 依式(2-4),利用操作A、B、C、D的數據,lgv對 作圖,可得一直線,斜率即為m。同理,利用操作D、E、F的數據,lgv對lgc(I-)作圖,可計算得n。再由m和n,從而得到反應級數m+n。
作圖,可得一直線,斜率即為m。同理,利用操作D、E、F的數據,lgv對lgc(I-)作圖,可計算得n。再由m和n,從而得到反應級數m+n。
數據處理:m=________;n=________。
通過計算得到m和n,代入式(2-3),可以得到速率常數k,將得到的k填入表2-4。
表2-4 反應級數和反應速率常數的計算
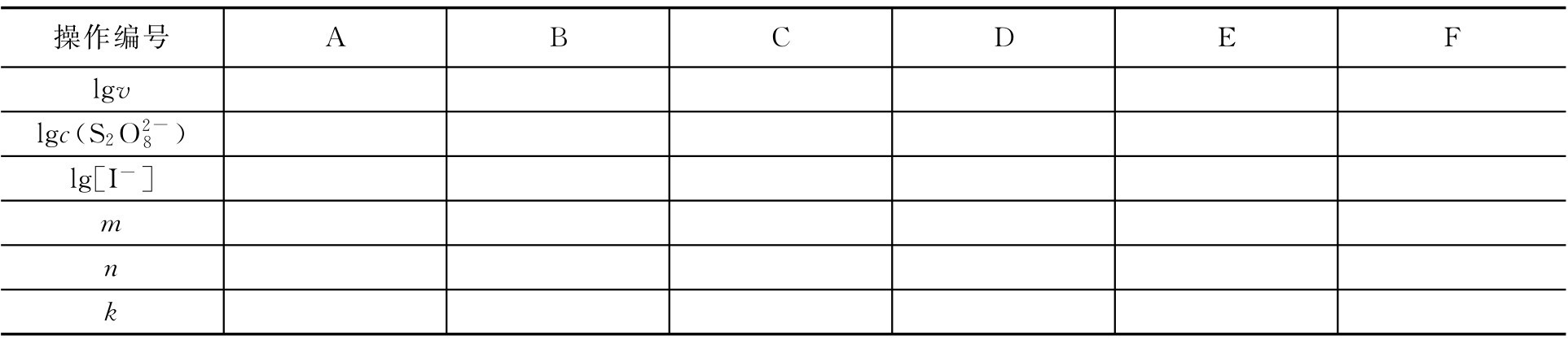
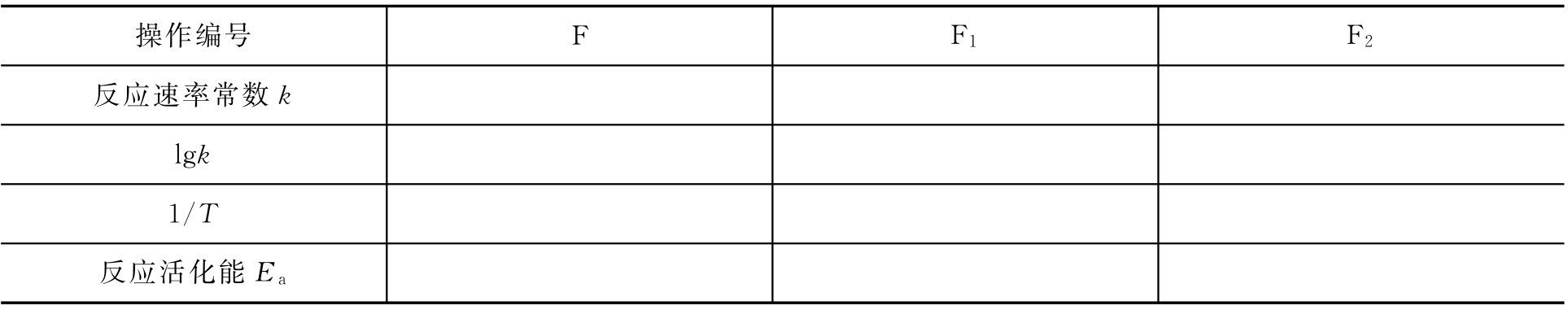
②反應活化能的計算 利用式(2-5),求得不同溫度下的k,以lgk對1/T作圖得一直線,此直線的斜率為 ,由此可以計算反應活化能Ea,數據填入表2-5。
,由此可以計算反應活化能Ea,數據填入表2-5。
表2-5 反應活化能的計算
(3)操作結論
①增加反應物的濃度,使反應速率________,反之亦然。
②升高溫度使反應速率________,反之亦然。溫度對反應速率的影響比較顯著。
范特荷夫經驗性的近似規則:一般反應溫度每升高________,反應速率增大到原來的________倍。
③合理使用催化劑,使反應速率________。
6.問題與思考
(1)用實驗結果說明,根據反應方程式,是否能確定反應級數?________。
(2)本實驗如何得到化學反應級數?________。
如何得到反應速率常數和反應活化能?________。
(3)若不用 ,而用I-或I3-的濃度變化來表示反應速率,則k值是否一致?________。
,而用I-或I3-的濃度變化來表示反應速率,則k值是否一致?________。
(4)對于任務材料中的反應液,________的量必須準確量取。
(5)操作中因為________可以由出現藍色的時間長短來計算反應速率。溶液出現藍色后,反應是否終止?________。
(6)下列操作對結果有何影響?
①取6種試劑的滴管沒有分開專用,對結果的影響是________。
②先加入(NH4)2S2O8,最后加入KI溶液,對結果的影響是________。
③慢慢加入(NH4)2S2O8溶液,對結果的影響是________。
④溫度不恒定,對操作結果的影響是________。
(7)本操作Na2S2O3的用量過多或過少,對結果的影響是________。
2.1.3 知識寶庫 化學反應速率
1.化學反應速率的概念及表示方法
化學反應速率是在一定條件下,衡量反應物轉化為生成物快慢的物理量,可用單位時間內反應物濃度的減少或生成物濃度的增加來表示。
濃度單位以mol/m3、mol/L表示,時間單位可以是秒(s)、分(min)、時(h)。因此,反應速率單位一般為mol/(m3·s)、mol/(L·s)。
實驗證明,多數化學反應都不是勻速進行的,在整個反應過程中,反應速率是個變量。按照所選時間間隔長短不同,化學反應速率可分為平均速率和瞬時速率。
(1)平均速率
平均速率為在一定時間間隔內求得的反應速率,用 表示。
表示。

式中,Δc/Δt為在時間間隔Δt=t2-t1內反應引起反應物或生成物濃度改變Δc=c2-c1,因為反應速率總是正值,所以用反應物濃度的減少來表示時,上式右邊取負號。若用生成物濃度的增加來表示時,上式右邊取正號。
一般反應: aA+bB qC+pD
qC+pD

原則上,可以用參加反應的任何一種物質的濃度變化來表示反應速率,但一般采用濃度變化易于測定的那種物質。
(2)瞬時速率
平均速率是討論一段時間間隔內的速率,而在這段時間間隔內的每一時刻,反應速率是不同的。因此,要確切地描述某一時刻的反應快慢必須將時間間隔盡量減小,當Δt→0時,此時的反應速率就是這一瞬間反應的真實速率,稱為瞬時速率v。

瞬時速率必須用作圖法求得。由于瞬時速率真正反映了某時刻化學反應進行的快慢,所以比平均速率更重要,有著更廣泛的應用,故以后提到反應速率,一般指瞬時速率。
2.影響反應速率因素
(1)濃度對反應速率的影響
①基元反應和非基元反應 大量事實表明,絕大多數化學反應并不是按照反應方程式一步完成的,而往往是分步進行的。一步完成的反應稱為基元反應,由一個基元反應構成的化學反應稱為簡單反應;由兩個或兩個以上的基元反應構成的化學反應稱為非基元反應或復雜反應。
人們常把決定整個反應速率的那步反應稱作控制步驟或定速步驟。因此,掌握了反應機理,就可抓住定速步驟的反應速率及其影響因素,對癥下藥地解決反應速率問題。
②反應分子數 反應分子數是從微觀上說明各反應物分子經碰撞而發生反應的過程中所包括的分子數。因此,反應分子數僅對基元反應而言。按反應的分子數,基元反應可分為單分子、雙分子和三分子反應三類,絕大多數基元反應屬于雙分子反應。
③速率方程和速率常數 為什么增大反應物的濃度會使反應速率加快?恒溫下的化學反應速率,主要決定于反應物濃度。濃度越大,反應速率越快。這一事實可用“有效碰撞理論”加以解釋。在一定溫度下,反應物分子中活化分子百分數是一定的,所以增加反應物濃度,單位體積內活化分子的數目增大,反應物分子間的有效碰撞機會增多,反應速率加快。其定量關系為:
aA+bB qC+pD
qC+pD
v=kcm(A)cn(B) (2-6)
式中,m和n值由實驗確定;v是瞬時速率。
a.對于基元反應:m=a,n=b
v=kca(A)cb(B) (2-7)
式(2-7)稱為反應速率方程,表示在基元反應中,化學反應速率與反應物濃度冪的乘積成正比,其冪的方次等于反應方程式中相應物質的計量系數,這一規律叫做質量作用定律,式中k稱為反應速率常數。
對某一反應,在一定溫度下,k為常數。溫度改變,k隨之改變。但反應物濃度的改變不會影響k值。
b.對于非基元反應,一般來說:m≠a,n≠b,m和n值由定速步驟確定。例如:
2NO+2H2 N2+2H2O
N2+2H2O
是非基元反應。
該反應分兩步進行:
2NO+H2 N2+H2O2(慢反應) (2-8)
N2+H2O2(慢反應) (2-8)
H2O2+H2 2H2O(快反應) (2-9)
2H2O(快反應) (2-9)
所以,總反應速率由第一步慢反應決定,其速率方程式為:
v=kc2(NO)c(H2)
這種定量關系是由實驗確定的。
④反應級數 在速率方程式中,反應物濃度的方次稱作反應級數。例如式(2-6)中對于A物質來說是m級反應,對于B物質來說是n級反應,m+n為反應總級數。某物質的反應級數越高,表明該物質濃度對于反應速率的影響程度越大。反應的總級數為1的化學反應叫做一級反應;反應的總級數為2的化學反應叫做二級反應,以此類推。
(2)溫度對反應速率的影響
溫度是影響化學反應速率的重要因素,實驗表明:溫度每升高10℃,反應速率增加2~4倍。為什么升高溫度會使反應速率加快?溫度升高,分子的運動速率加快,單位時間內分子間的碰撞次數增多,所以反應速率加快。但是,根據氣體分子運動論的計算,溫度每升高10℃,分子在單位時間內的碰撞次數僅增加2%左右,顯然碰撞次數的增加不是反應速率加快的主要原因。更重要的是溫度升高,分子的能量普遍增大,此時,有更多的普通分子獲得了能量成為活化分子,提高了活化分子的百分率,使單位時間內分子間的有效碰撞次數顯著增多,因而反應速率大大加快。溫度對反應速率的影響程度比濃度要大得多。
①阿侖尼烏斯公式 從速率方程來看,溫度對反應速率的影響,主要體現在對速率常數k的影響上。溫度升高時,k值增加,反應速率相應加快。
1889年,瑞典化學家阿侖尼烏斯提出下列經驗公式:

式中,k是速率常數;e為自然對數的底數(2.718);A稱為指前因子或頻率因子;Ea為活化能;R是理想氣體常數,8.314J/(mol·K);T是熱力學溫度;指數-Ea/RT的分子分母都是能量單位,所以指數項本身無量綱,A的單位與k相同。
阿侖尼烏斯公式較精確地反映了反應速率與溫度的定量關系。對于某指定的化學反應,活化能Ea可視為一個定值(一般情況下,A和Ea不隨溫度而變化),速率常數僅決定于溫度,由于k和T的關系是一個指數函數,T的微小變化將會引起k值較大的變化。
將式(2-10)兩邊同時取對數:

由公式可以看出:
溫度升高,k值增大,反應速率加快;
對于不同的化學反應,當溫度一定時,活化能越小,k值越大,反應速率越快;反之,活化能越大,k值越小,反應速率越慢,而且活化能較大的反應,其反應速率隨溫度的增加較快,所以升高溫度對活化能較大的反應更有利。
②阿侖尼烏斯公式的應用 主要應用包括:求反應活化能;求速率常數。
(3)催化劑對反應速率的影響
①催化劑和催化作用 催化劑是指能顯著改變化學反應速率,其本身的化學組成和質量在反應前后均不改變的物質。催化劑能改變反應速率的作用稱為催化作用。
凡能加快反應速率的催化劑叫正催化劑,減慢反應速率的催化劑叫負催化劑(或阻化劑)。一般提到催化劑均指正催化劑,如合成氨用的鐵粉、制備SO3用的V2O5等都是正催化劑;而橡膠防老劑、金屬緩蝕劑、化肥穩定劑等都是負催化劑。
有些物質本身沒有催化作用,若把它加到催化劑中,卻能使催化劑的催化活性顯著增大,這類物質稱為助催化劑,例如合成氨的鐵催化劑中,加入少量的Al2O3和K2O,可使其催化活性增大10倍,Al2O3和K2O就是助催化劑,還有一些物質,即使很少量的混入催化劑中,也會使催化劑的活性急劇降低或完全消失,這種現象叫催化劑中毒。引起催化劑中毒的物質叫催化劑毒物。硫化物、一氧化碳等都是合成氨催化劑的催化劑毒物。因此,合成氨所用原料氣必須經過脫硫凈化等處理過程。
反應中也有不需要另加催化劑而能自動發生催化作用的。例如,硝酸經過處理除去氮的氧化物之后,投入銅片,最初幾乎不發生反應,但當反應中有少量NO或NO2生成時,反應速率會突然加快,這種作用稱作自催化作用。
②催化原理 催化劑為什么能加快反應速率?許多實驗結果表明,催化劑之所以能加快反應,是因為它參加了反應過程,改變了原來反應的途徑,降低了反應活化能。催化劑對反應速率的影響要遠大于溫度和濃度。
③催化劑的基本性質
a.催化劑雖然參與反應過程,但在反應前后它本身的組成和質量保持不變。
b.催化劑只能加速熱力學認為可能發生的反應,對于熱力學計算不能發生的反應,使用任何催化劑都是徒勞的。催化劑不影響反應物和生成物的相對能量,不改變反應的始態和終態。因此,催化劑只能改變反應的途徑,而不能改變反應發生的方向和程度。
c.催化劑具有特殊的選擇性。一是某種催化劑常對某些特定的反應有催化作用,例如鐵粉是合成氨的特效催化劑,它對SO3的制備反應卻是無效的。二是同樣的反應選用不同的催化劑,可能進行不同的反應。例如,乙醇的分解反應,選用不同的催化劑可以得到不同的生成物。

根據這一特性,可由簡單易得的原料,采用不同催化劑制得多種產品。
d.對于可逆反應,催化劑能同等程度地加快正、逆反應速率。在一定條件下,正反應的優良催化劑必然也是逆反應的優良催化劑。例如,鐵催化劑能加速氨的合成,也能加速氨的分解。